Заповядайте в нашия форум - www.dentalforum-bg.com или следвайте връзката за директен вход във форума...
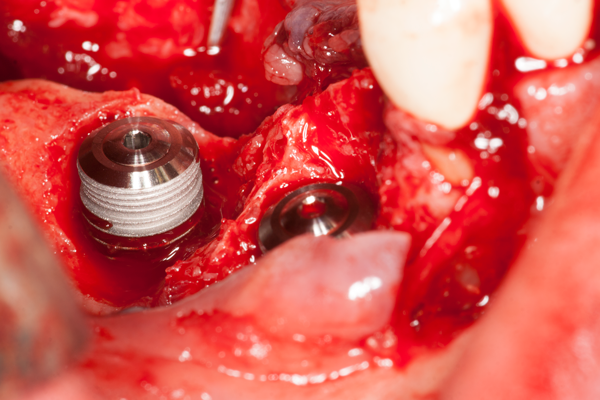
Един от най-лесните случаи на костна пластика и в същото време един от най-честите като приложение - изграждане на кост около поставен зъбен имплант. Това се налага поради факта че за да бъде функционално годен, всеки един зъбен имплант е необходимо да бъде заобиколен от костна тъкан с дебелина поне 2 милиметра.
Костна пластика с автогенна кост
За възстановяване на долната челюст може да се използва трансплантат от ребро. Той се взема по-лесно, оперативната намеса е по-атравматична и не ограничава подвижността на пациента в постоперативния период. Може да се вземе в достатьчна дължина и при нужда повече от едно ребро. При единично ребро се предпочита VII ребро. При заместване на екзартикулиран участьк от челюстта ребреният трансплантат се взема с хрущялен сегмент за заместване на ставата. Извършва се разрез по дължината на реброто. Периостьт се срязва надлъжно с Т-образен разрез, депериостира се с ребрен разпатор и се срязва с костотом в необходимата дължина. Периостът, мускулите и кожата се зашиват послойно. С течение на времето периостьт възстановява отнетия фрагмент. При отслояването трябва да се върви строго субпериостално, за да се избегне нараняване на париеталната плевра.
Много автори (Львов, 1923; Лимберг, 1942; Александров, 1955; Longacre – De Stefano, 1957) препоръчват използуването на разцепен ребрен трансплантат, предложен за първи път от Brown(1917). При този метод се взема само повърхностната кортикална пластинка заедно сьс спонгиоза, като дълбоката остава, с което не се прекъсва континуитетът на реброто. При определени показания (покриване на черепен дефект, двустранна остеопластика на долната челюст, контурна пластика при лицева асиметрия) се практикува вземане на цял трансплантат и разцепването му с използуване на двете половини самостоятелно. С подходящ сепаратор се срязва предната кортикална мастинка на окола 1 мм. от страничните ръбове и напречно в двата края на трансплантата, след което заедно с периоста фрагментът се отцепва от задната кортикална пластинка с жлебовидно длето. Според авторите разцепеният ребрен транспланатат прираства по-лесно и е по-устойчив.
Зъбни импланти Имплантатни системи Цени на зъбните импланти Лицево - челюстна хирургия Лимфен възел
Трансплантатът от тибия представлява трансплантат от компактна кост, който се използува от някои автори най-вече за оформяване на носния скелет. Използва се все по-рядко в лицевата пластика поради временната инвалидност, която предизвиква, и по-трудното захранване на трансплантата, свързано с бедната му васкуларизация. Трансплантатьт се взема с дъговиден разрез по медиалната повърхност на тибията. С циркулярен срез или с длето се отцепва необходимият костен шпан от предния ръб на костта. Трансплантатът се взема заедно с периоста, който го предпазва от евентyално фрактуриране.
В последните години се прилага възстановяване с костни фрагменти от разстояние, изискващо микрохирургична техника. Преди да се прекъснат съдовете на фрагмента се подготвя реципиентната ложа и съдовете за включване. За предпочитане е използване на съдове с еднакъв калибър. При идеални условия анастомозата е термино - терминална или термино - латерална. Термино - терминална анастомоза се извършва като след клампиране на двата края на всеки съд (на донорската и реципиентната област) се отпрепарират адвентициите с пинсета. Излишъкът от адвентиция се изрязва и съдовете се промиват отвътре. Поставянето на първия шев е най-трудно, като възлите трябва да стоят извън съда. Термино-латeралната анастомоза е по-трудно изпълнима и включва изрязването на отвор в реципиентния съд, към който трябва да се зашие другият съд.
www.dentalimplants.bg www.ralev-dental.com www.bg-dentist.info www.sliven-dental.info
Костна резорбция Пиринwww.oralsurgery.bg Базални импланти www.ralev-dental.bg www.bg-tourinfo.com Методи за костна пластика в имплантологията
Фибуларното артериализирано ламбо има все по-често приложение за реконструкция на мандибулата. То притежава здрава компактна кост, която може да носи тежест. При възрастен индивид е възможно да се вземе до 22 см. кост. Съдовете са с голям калибър и са константни. Могат да се използват всички видове ламба - костни, остеокутанни, остеомиокутанни и костно - мускулни. Последствията за донорския участьк са минимални. Изхранващ съд е а. рeronеа, която е външен клон на бифуркацията на тибиоперонеалния ствол. На ниво горна и средна трета (15 – 27 см. от главата на фибулата в интермускуларния септум между m. peroneus longus и m. soleus се намират няколко (4 до 7) септокутанни перфорантни съда, които трябва да се запазят ако е необходима кожа за ламбото. Те могат да изхранват кожна територия с размер 22/14 см. Венозната система е паралелна на артериалната. От началото на a. peronea до първите клонове, предназначени за фибулата, може да се образува съдов педикул с дължина от 3 - 5 см. Анатомичното разположение на съдовете позволява да се повдигне фасциокутанно ламбо на проксимално или дистално краче. На практика най-голямо приложение има свободното костно или остеокутанно ламбо.
Преди нанасянето на разреза се маркират главата на фибулата и страничният малеол. Необходимата кост се изчислява с по 2 см. повече от всеки край. Проксималната остеотомия трябва да се планира дистално на поне 8 см. от главата на фибулата, за да не се увреди n. peroneus соmmunis. Дисталната остеотомия трябва да запазва дисталната четвърт на фибулата, за да не се наруши стабилностга на стъпалото, най-малко на 5 см. от малеола. Кожните инцизии се маркират и кракът се обезкръвява с пневматичен Есмарх до 300 мм. Hg. За костно - мускулно ламбо кожният разрез се прави по задния ръб на фибулата. Мm. реronei заедно с n. peroneus communis се ретрахират напред, а m. soleus назад, така че се експонира интермускуларната фасция между тях и тя се инцизира. Трябва да се идентифицира и лигира дисталният край на перонеалната артeрия. Взима се костта с периоста. Включват се до 1 см. от мускулите, които се захващат за него. Междукостната мембрана се разцепва от дистално към проксимално. Последна се прави проксималната остеотомия.
Щифтово изграждане Имплант Колагенови мембрани Зъбни импланти Избелване на зъби Базални импланти
България Върхове в България Сепсис - тежък патологичен процес Синтетичен костозаместител Лимфен възел
При деца може да се вземе горната епифиза на фибулата, което позволява прехвърляне на растeжен хрущял, но трябва да се има предвид, че епифизата се храни главно от а. tibialis аnterior. Може да се включи и n. saphenus externus за ресенсибилизиране на ламбото. Донорският участьк се покрива сьс свободна кожа при размер над 8 см. Неудобствата на това ламбо са свързани с риск от лезия на n. peroneus communis. Възможни са и нарушения в стабилността на стьпалото с отлепване на m. flexor hallucis longus и m. tibialis роsterior, особено при деца.
Васкуларизирано ламбо от crista iliaca е описано през 1974 година. То предоставя едни от най-добрите възможности за реконструкция на мандибулата. В ламбото може да се включи кост, мускул и кожа. Крилото на илеума има извит ход, който много наподобява на мандибулата. Изхранващият съд е а. сircumflеха iliaca рrofunda, която е клон на а. iliaca externa. Повдигането на ламбото започва с очертаване на кожните граници и откриване на феморалните сьдове. След това се търсят а. circumflеха iliaca superficialis и а. epigastrica inferior superficialis. После се повдига ингвиналният лигамент и на около 2 см. под него се открива а. circumflexa iliaca рrofundа. Дисекцията продължава по горния ръб на ламбото, като се прерязват m. obliquus externus, m. internus и m. transversus. Желателно е да се фиксират кожата и мускулите към кожата на ламбото. Костта се прерязва от латерално към медиално и може да се моделира според конкретните нужди. За реконструкция на мандибулата обикновено съдовете се включват към а. et v. temporalis superficialis.
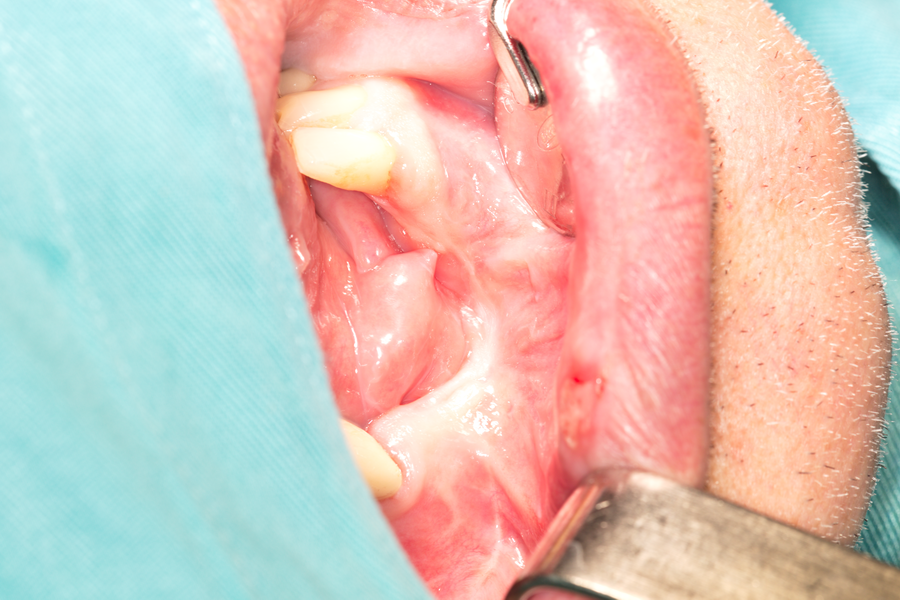
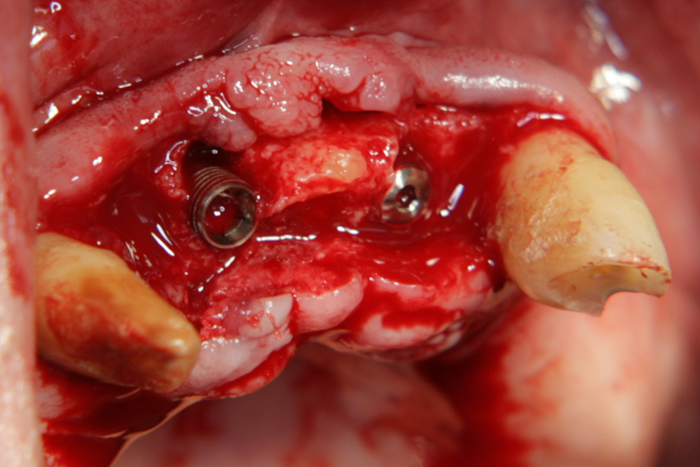
Случай на тежка атрофия на фронталния участък на долна челюст вследствие фрактура - некротизирал е фрагмент, съдържащ три долни резеца - два централни и един страничен вляво. Случаят подлежи на костна реконструкция независимо дали ще се поставят зъбни импланти или ще се изработва мостова протеза - налице е ясно изразено хлътване, която ще наруши естетиката и най-вече хигиената на устната кухина при този пациент. Съществува известна възможност хлътването да се компенсира с изработка на мостово тяло с екстензия от розова керамика, която би дала донякъде естетичен резултат; под това мостово тяло обаче биха се задържали хранителни остатъци, която ще се почистват от пациента изключително трудно - реално най-долната част на това своеобразно седло и на 5 мм. под нивото на пода на устната кухина. Поради това и преценихме че е необходимо да се осъществи костна пластика.
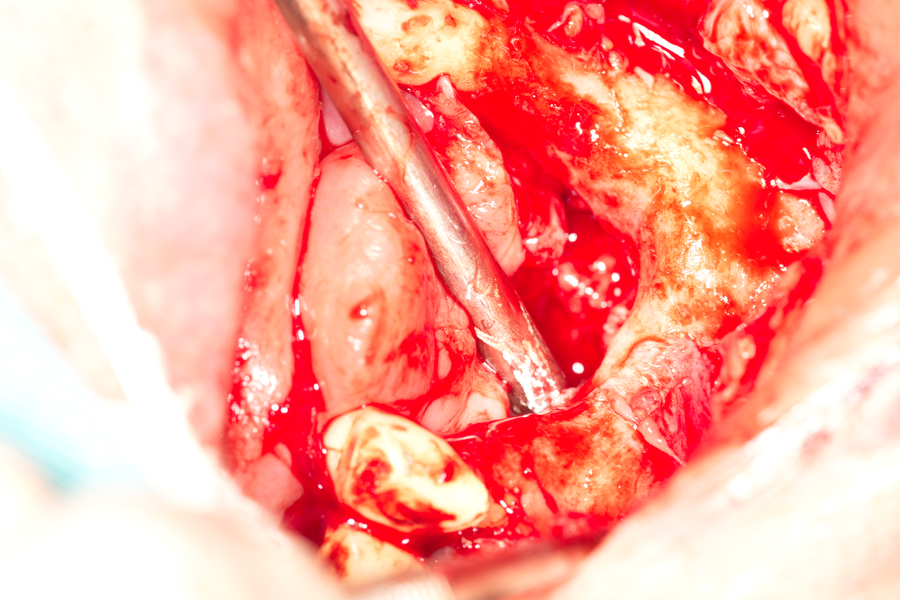
Реципиентната ложа след отпрепариране на меките тъкани. Вижда се плътна и здрава компактна пластинка, която не е добра основа за приемане на трансплантата - тя самата е слабо кръвоснабдена и не е добър източник на остео- и фибробласти. Поради това е необходимо да се перфорира многократно - отворите в кортикалиса стават източник на костни клетки и костни морфогенетични протеини, кървоносни съдове и фибробласти, които се стремят да регенерират костта в областта на дупчиците. Същевременно обаче те намират отлични условия за развитие около автогенния трансплантат и водят до образуване на нова кост - поради което и перфорациите се прилагат изключително често при необходимост от костна пластика.
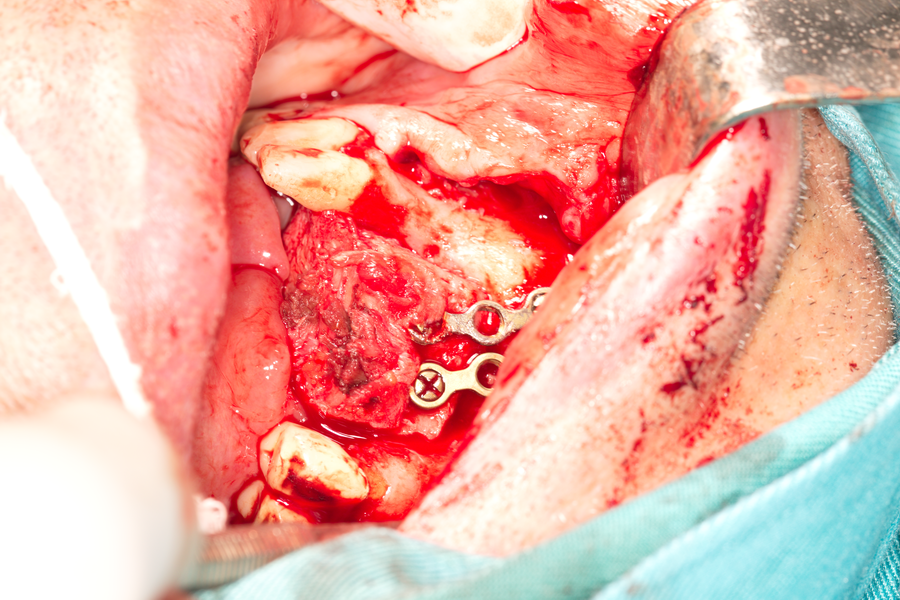
Поставен е автогенен костен трансплантат - в случая донорското място е илиачният гребен на пациента. Фиксирането е извършено с две пластини за остеосинтеза
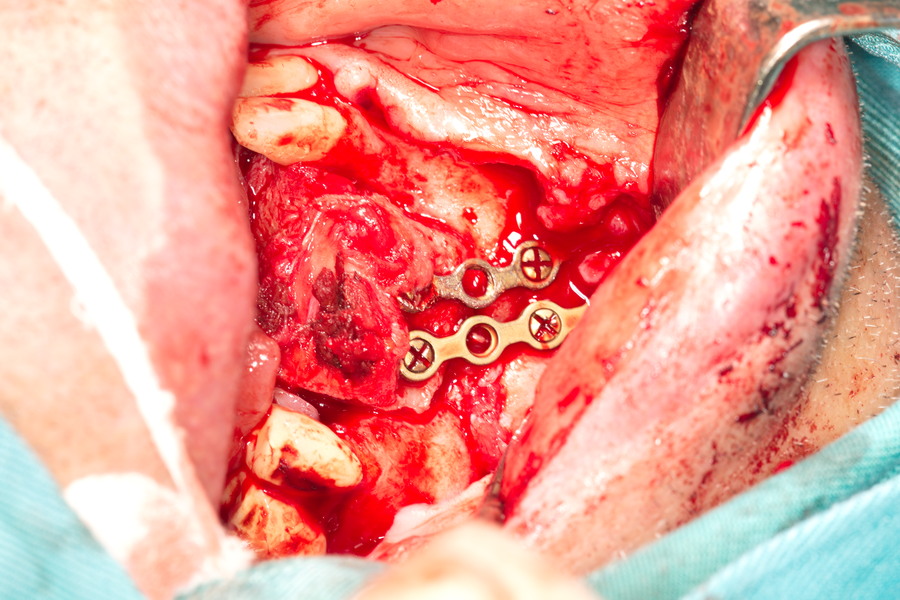
Имобилизация на трансплантата - тя е ключова за протичането на добър заздравителен процес. Ако трнасплантатът е подвижен, се нарушава неговата реваскуларизация и започва резорбция. Много скоро след това не остава и следа от трансплантата - той се резорбира напълно. Като вече стана въпрос, скоростта на реваскуларизацията е 1 линеен милиметър на ден - следователно трансплантат като на снимката горе би следвало да бъде добре кръвоснабден след около 20 - 25 дни. Което и се получи на практика. Умишлено трансплантатът не е почистен от мускулната тъкан - според нашия клиничен опит истинските проблеми се създават не от епитела, а именно от мускулната тъкан. Тя има свойството да епителизира спонтанно, да сраства със съседна съединителна тъкан и периост, да фиброзира - което е всичко останало, само не и това, от което имаме нужда - образуването на костна тъкан. Веднъж интерпониран мускулен фрагмент между два костни фрагмента води до нулева консолидация на костта - образуват се само фиброзни мостове. Всичко това е формирано с течение на еволюцията - всички живи организми са подложени на всякакви травми и колкото по-бързо се регенерира разкъсаният мускул, толкова по-големи са шансовете на целия организъм за оцеляване. Поради всички тези фактори не почистихме залавното място на мускула към костния фрагмент по билото на гребена и в същото време отстранихме всякакви влакна между реципиентната ложа и трансплантата. Така мускулът остана като своеобразна биологична превръзка, покриваща трансплантата. Тя бързо успя да епителизира и да предпази подлежащата кост от проникване на инфекция в дълбочина, от замърсяване с хранителни остатъци и последващ разпад - известно е че епителът има отлична бариерна функция в целия организъм.
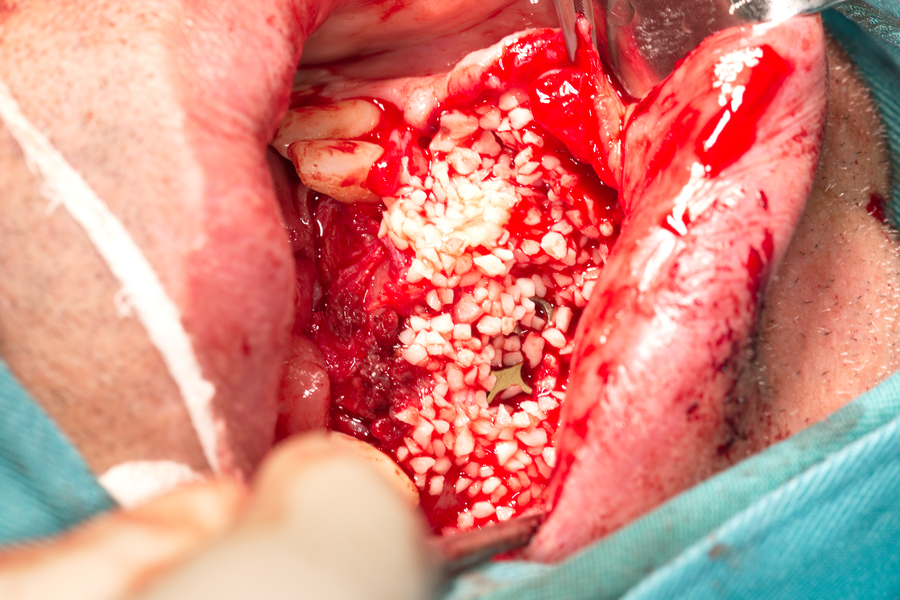
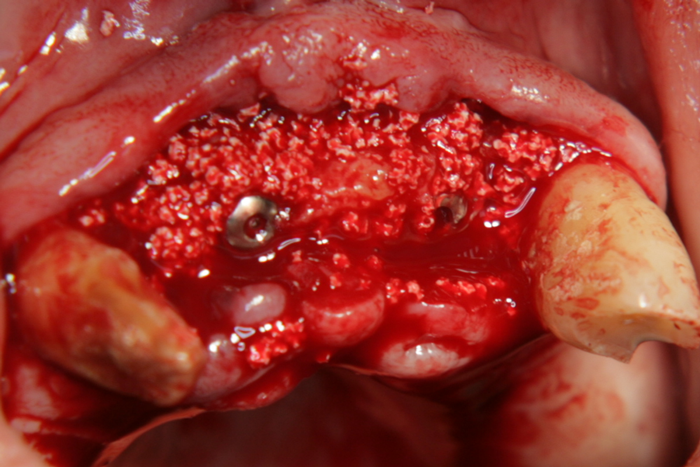
Допълнително около автографта бяха поставени гранули от ксенотрансплантат - говежда кост. Те ще се резорбират почти напълно, но ще станат и източник на минерализация за бъдещата новообразувана кост в организма в реципиентната ложа. Отново ключово значение има имобилизацията на трансплантата. Относно размерът на трансплантата - по литературни данни реваскуларизация е възможна при размер до 7 см. При по-голям линеен размер в най-дългото измерение на трансплантата се засилват рисковете от резорбция и е необходимо да се вземе предвид поставянето на васкуларизиран трансплантат.
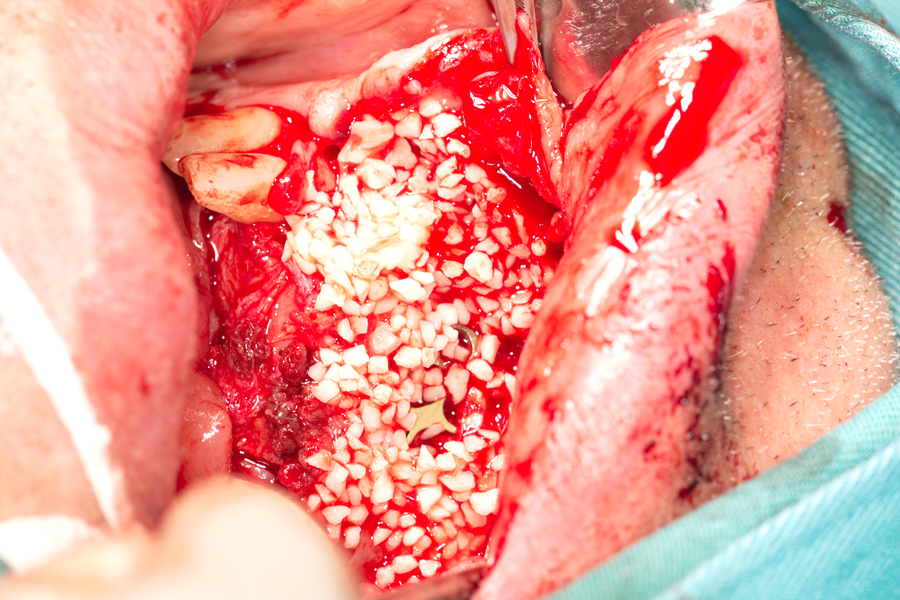
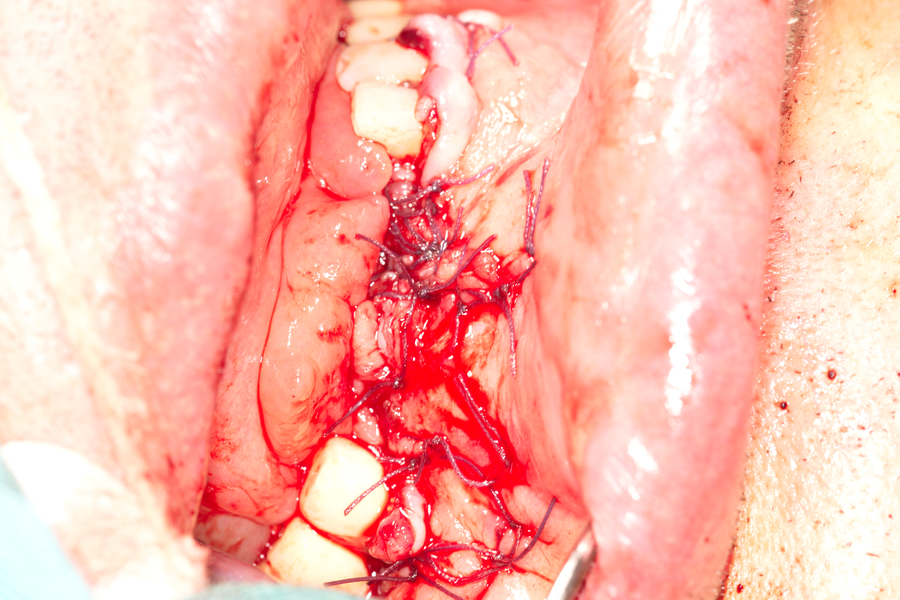
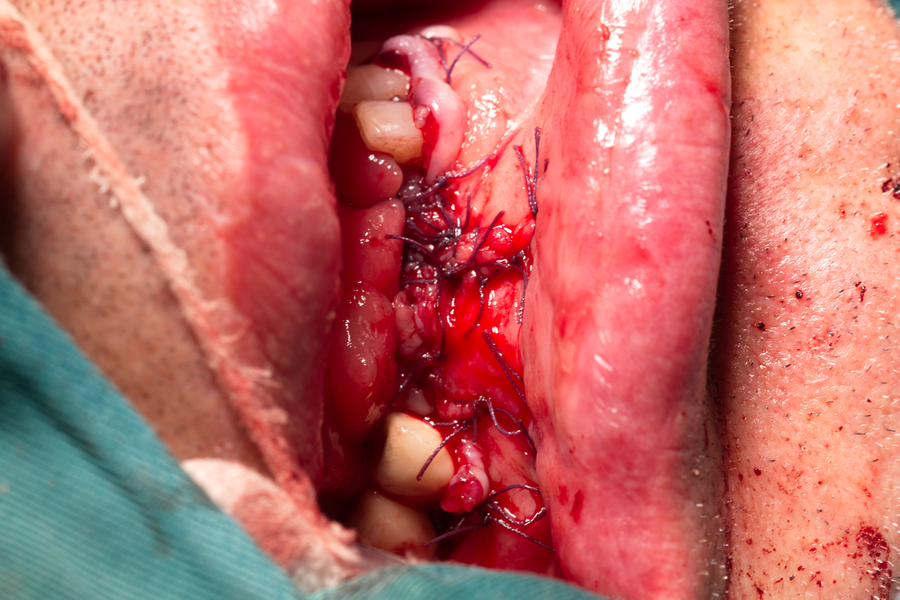
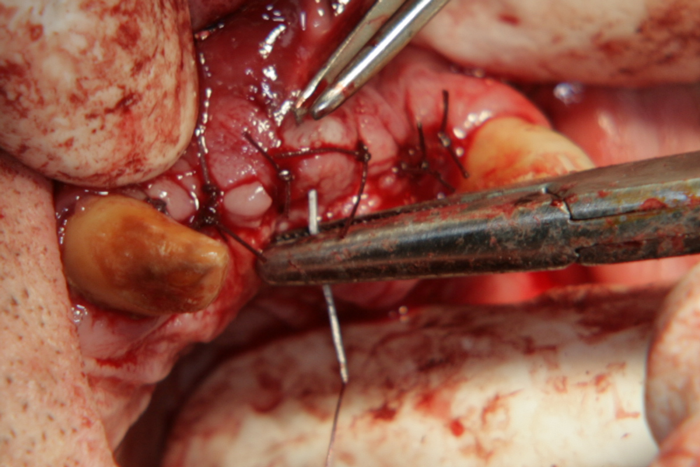
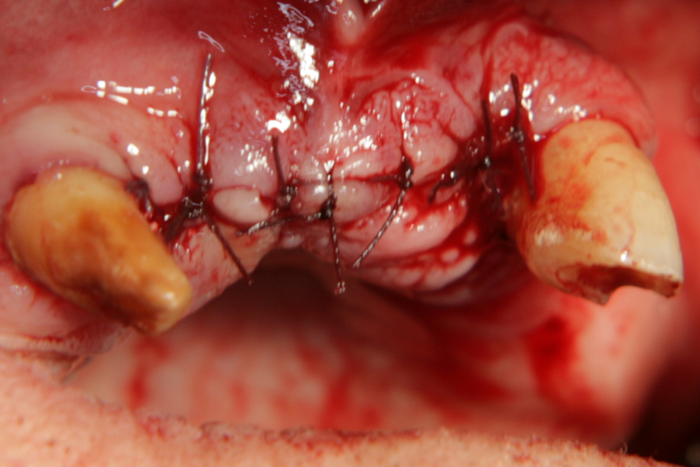
Меките тъкани са зашити плътно с голям брой конци и раната е херметизирана
При сравнителна преценка автотрансплантатът има винаги преимущества пред хомотрансплантата. В костната пластика на лицето автотрансплантацията е метод на избор поради относителна неголемия размер на необходимия фрагмент. Въпреки това хомотрансплантацията понякога намира своите показания. Някои автори (Плотников използуват хомопластиката и при остеопластичното възстановяване на долната челюст. Според него тя има преимущества в детска и старческа възраст, при системни поражения на костите и поради възможността да се използва за трансплантация лиофилизиран фрагмент или цяла долна челюст. Последната най-добре съотвества по форма на дефектния учасгьк, особено при възстановяване на ъгъла и възходящия клон при широка резецирана или екзартикулирана челюст. Други преимущества на хомотрансплантацията са липсата на допълнителна травма на пациента и възможността хомотрансплантатьт да се консервира и складира за бъдеща употреба. При хомотрансмантацията костта се възстановява от елементите на реципиентната повърхност и включените в нея костни и метаплазиращи клетки, като трансплантатът постепенно се резорбира и неорганичните му елементи се използват ката градивен материал за новообразуващата се кост. Едновременно с това разпадните му продукти действуват стимулиращо за костообразуването. Като отрицателни страни на хомотрансплантата са описани значително по-бавното костообразуване и предизвиканата имунобиологичната реакция.
Костна пластика с лиофилизирана кост
Консервиран материал се набавя най-често от пресни трупове, починали в резултата на травми или сърдечно - съдови заболявания с неинфекциозен характер на възраст от 18 до 45 години. Материалът се взема в стерилна обстановка и се консервира в тъканна банка чрез замразяване или лиофилизация. Последната се постига чрез изсушаване във вакуум при температура от - 40 ° до - 196 ° С. Лиофилизираният трансплантатат има снижени антигенни свойства и може да се съхранява при стайна температура практически неограничено време в стьклени херметически затворени банки или запоени ампули. Това позволява складирането му за използуване при масови бедствия. За нуждите на лицевата пластика се използуват лиофилизирана кост от гребена на илиачната кост, ребра, долна челюст, компактна кост от тибията или бедрото, лиофилизирани спонгиоза и костно брашно. Последните намират широко приложение за запълване на кистозни и други костни кухини или на цепнатини при оперативно раздалечаване на костни фрагменти. При възстановяване на големи костни дефекти се препоръчва комбиниране на хомо- с автотрансплантат. При приложение на лиофилизирана кост е необходимо да се спазва строга антисептика, тъй като такива трансплантати са много чуствителни към инфекции и при попадане на микроорганизми в оперативното поле бързо се стига до резорбция на трансплантата.
Костна пластика със синтетични материали
С развитието на съвременните остеокондуктивни и остеоиндуктивни материали приложение в костната пластика намира и алотрансплантацията. При нея се използват материали, които прирастват към костта или се резорбират бавно и на тяхно място се отлага нова кост. Приложение намират мадрепоровите корали и различни видове полимери, с които се запълват костни кухини с различни размери. При биорезорбируемите материали е добре да се прилагат бариерни мембрани за направлявана тъканна регенерация. Те не позволяват прорастване на епителни клетки към материала, което влошава резултата от интервенцията.
При всяка костна пластика е необходимо да се спазват определени изисквания. Трансплантатът се имплантира в здрави неинфектирани тъкани; обхваща се плътно от добре кръвоснабдена и в достатъчно дебел слой тъкан откъм устната кухина и кожната повърхност. Извършва се екзактна хемостаза, за да се предотврати образуването на хематом между трансплантата и реципиентната повърхност. Осигурява се достатъчно широк и плътен костен контакт между трансплантата и костните участъци на ложата. Задължителна е надеждната фиксация на трансплантата и имобилизацията на целия костен комплекс за избягване на движението в контактните пунктове.
Напоследък доста често се прилагат костни морфогенетични протеини, които осъществяват костна пластика на генетично ниво. С помощта на рекомбинантни ДНК-технологии са синтезирани различни фактори, като най-голямо приложение намира BMP-2 - костният морфогенетичен протеин тип 2. Той стимулира стволовите клетки да се диференцират в посока костни клетки. Подобни протеини се съдържат и в лиофилизираната кост, но в много малки количества и поради това последната е остеоиндуктивна в много малка степен. В по-висока концентрация тези протеини се съдържат в автогенната кост; все пак синтетичните препарати са силно концентрирани и се счита че индуцират образуването на нова кост на атипични места - дори при инжектиране в мускулите на животни. Костните морфогенетични протеини стимулират не само образуването на нова костна тъкан, но и ангиогенезата - образуването на съдове. Двата процеса така или иначе са интимно свързани - няма как да се формира нова кост без да прорастнат капиляри в трансплантат от какъвто и да е тип. BMP-2 стимулира растежа на ендотела, а остеобластите секретират васкуларен ендотелен растежен фактор А, който от своя страна допълнително подпомага растежа на кръвоносни съдове. Повечето проучвания, проведени върху животни и върху пациенти дават убедителни доказателства за ползата от прилагането на костно - морфогенетични протеини - новата кост е в по-голямо количество и с много по-добро качество в сравнение със случаите, при които не се прилага ВМР, а само синтетичен графт или ксенотрансплантат. За съжаление в малък брой случаи обаче се наблюдава склонност към развитие на неопластични процеси като следствие от неконтролируемата пролиферация на клетките, което за момента донякъде ограничава употребата на морфогенетичните протеини.
Приложение намира и обогатената с тромбоцити плазма, която се получава при центрофугиране на венозна кръв, взета от пациента. Това е автогенен материал с отлични свойства, който може да се прилага самостоятелно или в комбинация с други остеопластични материали. При тази плазма материалът не се подлага на никаква термична или химична обработка (за разлика от лиофилизираните хомо- и ксенотрансплантати), при което не се губи остеоиндуктивния ефект на имплантирания материал. Установено е че самите тромбоцити съдържат голямо количество растежни фактори, които подтикват костта към растеж, матурация и минерализация. За богатата на тромбоцити плазма има вече натрупани доста проучвания - сравнени са методи за костна пластика с и без PRP. През 2012 година в International Journal of Craniomaxillofacial Surgery (брой 40: 409 - 415) е публикувана статия от швейцарски изследователски екип - Metzler, von Wilmowski, Zimmermann, Wiltfang und Schlegel. Авторите имплантират на животни фрагменти от периост, под който са поставени различни видове алопластични материали - говежда кост, корали и стъкло. За да се изключи остеогенното действие на локални протеини от собствената кост на пациента, взетият периост е имплантиран подкожно, в участък в който няма никакви костни тъкани, при което се цели да се проследи остеоиндуктивното действие на различните видове материали за костна пластика. Резултатите са донякъде неочаквани - богата на тромбоцити плазма изглежда има силно активиращо действие върху клетките на периоста и при апликацията на PRP се формира нова кост на атипични места. При имплантиране подкожно само на периост и алографт нова кост не се образува - формира се фиброзна тъкан, в която се разполагат зърната на остеопластичния материал. Като референтен материал служи автогенна кост, имплантирана подкожно - тя остава там непроменена и витална за периода на проучването (24 седмици). Авторите попадат и на друг интересен факт: най-вече при комбинация от Bio-Oss (Geistlich Biomaterials - Switzerland) и богата на тромбоцити плазма се формира нова кост. При тази комбинация степента на минерализация е 63.61 %. При приложение на периост и Bio-Oss без плазма степента на минерализация спада двойно и се наблюдава само в степен 32.41. При приложение на Algipore и богата на тромбоцити плазма се наблюдава минерализация в степен 34.37 %. При липса на плазма минерализацията е нулева. Никаква минерализация не настъпва при апликацията на биостъкло - търговската марка на продукта е Biogran, независимо дали е добавена PRP или не. В контролната група - при имплантирана автогенна кост - степента на минерализация е 89.88 %.
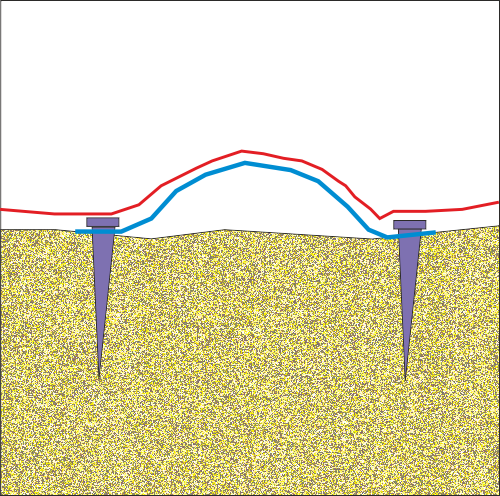
Клиничен случай, при който има нужда от костна пластика - между зъбния имплант и костта на горна челюст има цепнатина, която цепнатина трябва да се изпълни с костна тъкан, за да бъде лечението екзактно
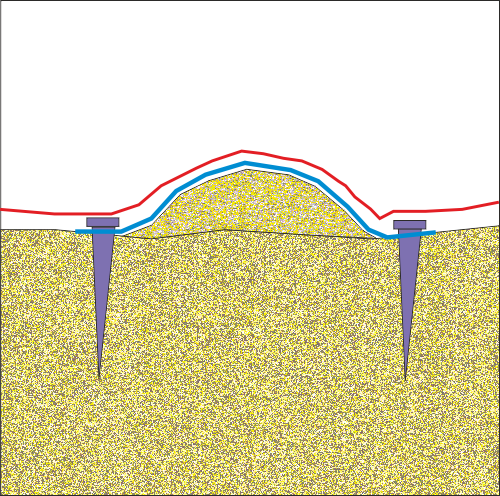
В областта на оперативното поле е поставен костозаместващият материал - бета-трикалциев фосфат
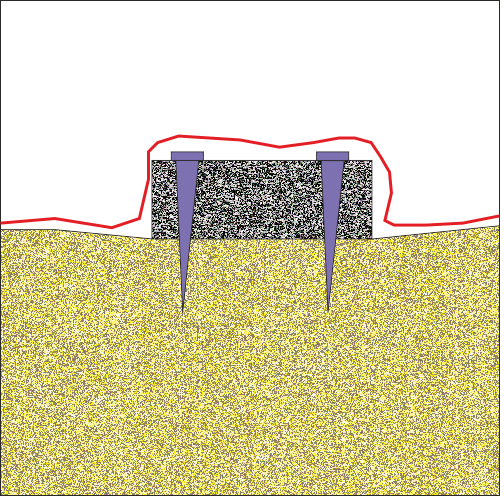
Оперативната рана е се зашива на глухо
Раната е зашита плътно, което е предпоставка за добър заздравителен процес. До момента все още няма единно мнение дали в този случай трябва да се поставя колагенова мебрана или не - според едната група автори това е задължително, защото мембраната предотратява навлизането на епителни клетки и хранителни остатъци в дълбочина; според други мембраната се явява излишна преграда за остеобластите от периоста, тъй като костта се регенерира предимно по периостален път. Във всички случаи обаче е необходимо да се изолира зоната на костната пластика от устната кухина - проникването на епителни клетки и хранителни остатъци в нея силно влошава постоперативния резултат. Адекватната костна регенерация е бавен процес, тъй като се изисква триизмерно възстановяване на костните тъкани; освен това е необходимо да бъде осигурена надеждна имобилизация на транплантата и чисто оперативно поле, без възможност за проникване в него на външни субстанции.
При всяка една костна пластика е от значение и как точно се обработва реципиентната ложа - мястото, в което се аплицира трансплантатът. Още от началото на развитието на лицево - челюстната хирургия се е прилагала обработка на костта с ротационен инструмент - диамамантено или твърдосплавно борче или фреза с различни форми. Тези ротационни инструменти обаче имат някои недостатъци - прекалено затопляне на костта, фрагментиране на костта, формиране на размазан пласт и нараняване на съседните меки тъкани. Всичко това води до забавяне на оздравителния процес и влошаване на резултатите от костната пластика. Поради това в последните години се прилага все по-широко обработката на костните тъкани с ултразвуков пиезотом - т.нар. пиезохирургия. При нея се използва апарат, който може да обработва костта с накрайници - те трептят с ултразвукова честота от порядъка на 24 - 32 kHz, при което изрязват и оформят костните тъкани. Върхът на апарата трепти и реже селективно минерализираните тъкани - не засяга меките тъкани и нервите по съседство. Освен това с ултразвуков пиезотом срезовете са доста по-прецизни и по-гладки, охлаждането е по-ефективно и като следствие видимостта интраоперативно е доста по-добра. Кървенето е доста по-малко, а срезните повърхности са доста по-гладки.
През януари 2018 година екип от италиански лицево - челюстни хирурзи (Alexandre Anesi et al, Journal of Craniomaxillofacial Surgery, Volume 46, Issue 1, January 2018) провежда проучване върху животни относно ефекта от срязване на костта с класически ротационен инструмент или ултразвуков пиезотом. Авторите нанасят няколко среза върху черепния покрив на зайци и проследяват оздравителния процес - след период от 15 дни. Резултатите са категорични - там, където разрезът е нанесен с ултразвуков пиезотом, оздравителният процес е много по-бърз. Съседните твърди тъкани са засегнати доста по-малко - в тях са налице много по-голямо количество витални остеоцити. Новообразуваната кост е доста по-плътна, има по-изразени трабекули, и доста по-голям модул на еластичност в сравнение с костта, която се образува след разрези с ротационен инструмент. Всичко това следва да се взема предвид при планирането на различни оперативни интервенции върху костните тъкани в лицево - челюстната област, а и в целия организъм изобщо.